Una reacción es un proceso químico en el cual las sustancias sufren una alteración en su estructura para así originar otras. El caso más usual y simple se da entre sustancias líquidas o gaseosas, o aquellas que se hallan en disolución; esto es así porque al estar más separadas permiten mayor contacto entre los cuerpos reaccionantes.
Existen, lógicamente, diferentes tipos de reacciones. En el caso de la reacción por sustitución, se trata de un tipo de reacción en la cual un átomo o un grupo de un compuesto químico son sustituidos por otro átomo o grupo. Esto significa que, a través de la reacción, un elemento reemplaza al otro en el compuesto; es a causa de esto que estas reacciones pueden llamarse también “de desplazamiento”.
Cuando se habla de grupo o, más bien, grupo entrante se hace referencia al conjunto de átomos que entran al sustrato, es decir, la molécula en la cual se lleva a cabo la sustitución. Los átomos expulsados, en cambio, se denominan grupo saliente. El resultado de la reacción de sustitución se llama “producto”.
Tipos de reacción de sustitución
Podemos distinguir dos tipos de estas reacciones: de simple sustitución y de doble sustitución. Veamos cada una:
- De simple sustitución: esta reacción se da cuando una sustancia simple entra en contacto con una compuesta y sustituye a uno de sus elementos.
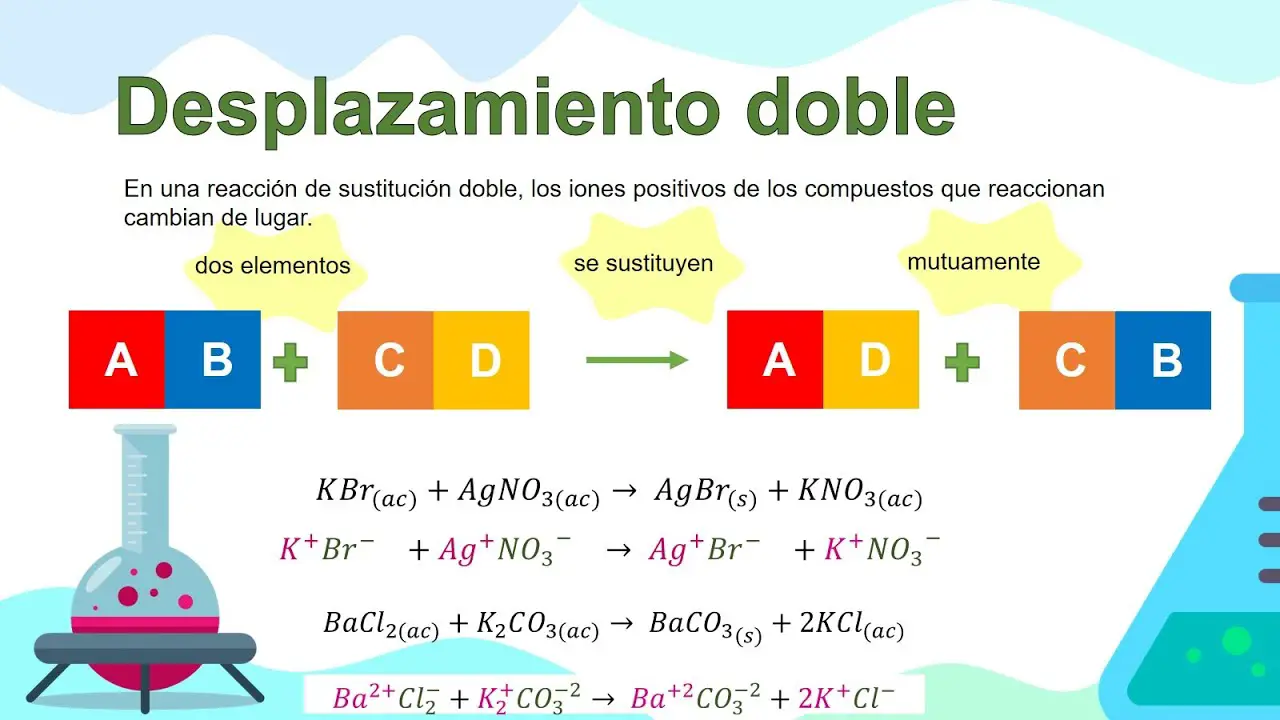
- De doble sustitución: también conocida como metátesis, se da entre dos compuestos distintos, los cuales terminan por formar una sustancia nueva. En estos casos, suelen intervenir compuestos iónicos en solución, por lo cual se produce un intercambio de cationes y aniones.
Además, las reacciones de sustitución, sean simples o dobles, pueden agruparse según su mecanismo en nucleofílica monomolecular o bimolecular.
- Sustitución nucleofílica monomolecular: es cuando la reacción se da por etapas en las cuales, primero se disocian los compuestos en iones y después, dichos iones reaccionan entre ellos.
- Sustitución nucleofílica bimolecular: la reacción se da de una sola vez: el ataque del reactivo y la expulsión del grupo saliente se dan al mismo tiempo.
Etapas de la reacción de sustitución
Existen 4 etapas en las que se divide la reacción de sustitución:
- Sustrato: se llama así a la molécula donde se realiza la sustitución.
- Reactivo o grupo entrante: así se llama al átomo o grupo de ellos que atacan al sustrato.
- Grupo saliente: es como se denomina al átomo o grupo de átomos expulsados del sustrato.
- Producto: se llama así al resultado de la sustitución del grupo saliente por el nucleófilo, en cuyo caso se habla de una sustitución nucleofílica.
Ejemplos
Un clásico ejemplo e reacción de sustitución se da al sumergirse cobre en nitrato de plata: el cobre expulsa a los átomos de plata, lo que origina un nuevo compuesto: el nitrato de cobre. También puede citarse la sustitución de bromo por cloro, lo que se puede expresar con la siguiente fórmula: Cl2 + NaBr -> NaCl + Br2
