
En este artículo explicaremos el concepto de la combustión, las etapas del proceso, ejemplos diarios de combustión y sus características.
Concepto de Combustión
La combustión es una reacción química, de velocidad rápida y de tipo exotérmica (reacciones que generan liberación de energía), que involucra a materia en estados heterogéneos (equilibrios de tipo sólido-gaseoso o gaseoso-líquido) , así como gaseosos. Al finalizar una reacción de combustión, se generará calor y luz.
Cómo se produce la combustión

Como indicamos anteriormente, la combustión involucra una reacción química de reducción-oxidación. Esto indica que en la reacción una sustancia se reducirá (ganará electrones) a través de la oxidación de otra (quién perderá electrones y los “cederá).
En la combustión, un agente oxidante, el oxígeno, también denominado comburente, obtendrá sus electrones a través del agente reductor, el combustible. Esta reacción se define como:
Compuesto A + O2 = Compuesto B + Co2 + H20 + Energía
Características de la combustión
En un análisis físico, la combustión es la oxidación de los combustibles. Por lo tanto, es necesaria la presencia de oxígeno para este tipo de procesos y, además, los combustibles se compondrán de sustancias volátiles o de fácil encendido en la oxidación, generalmente se constituyen de materiales como azufre, hidrógeno y carbono.
Si analizamos a la combustión desde un punto de vista químico, una combustión sería una reacción de Reducción-Oxidación, conocida como reacción Redox. Este tipo de reacción se genera de manera controlada en los procesos, sacando los casos accidentales de descontrol de energía. Además, al ser un proceso de intercambio de electrones, explica la generación de energía lumínica y térmica.
La combustión involucra siempre a un combustible (que es la sustancia que se consume para la reacción debido a sus propiedades) y a un comburente (que es la sustancia química que provoca la reacción), y puede generar productos de la combustión tales como vapor de agua, residuos sólidos del combustible consumido, así como también del comburente, y dióxido de carbono.
Tipos de combustión
- Combustión incompleta: El proceso de combustión se realiza de forma parcial, con productos a medio oxidar de los gases combustibles, pudiendo ser hidrógeno, monóxido y partículas de carbono.
- Combustión completa: En ellas la oxidación es total, se consume todo el material combustible y los subproductos son compuestos oxigenados: agua en forma de vapor, dióxido de carbono o azufre.
- Combustión neutra: También llamada estequiométrica, son combustiones completas ideales, realizadas en laboratorio que utilizan las cantidades exactas de oxígeno para una reacción perfecta (el oxígeno exacto se determina mediante cálculos estequiométricos de reacciones).
Etapas o reacciones de la combustión
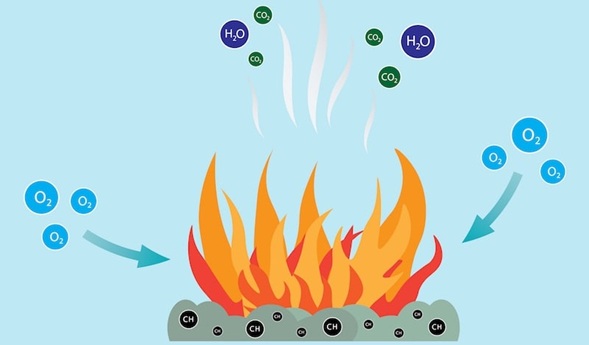
Los procesos de combustión incluyen estas etapas:
- Pre-reacción: Es la etapa en que los combustibles descomponen sus hidrocarburos para comenzar la reacción de combustión, a través de la formación de radicales (compuestos de alta inestabilidad molecular).
- Oxidación: En esta etapa el oxígeno comienza a reaccionar con los radicales libres, generando en el proceso la mayor parte de la energía calórica de la combustión. Debido a la reacción, se genera un desplazamiento rápido y descontrolado de electrones.
- Fin de la reacción: Sucede al finalizar el proceso de oxidación de radicales, así como de la conformación de gases y subproductos liberados al finalizar la reacción. Sucede cuando el combustible se consume en su totalidad.
Ejemplos de combustión
- Encendido de cocinas: El combustible es un gas hidrocarburo, que al contactar con el aire y la llama inicia la reacción,
- Encendido de fósforo: Al raspar la cabeza del fósforo, el azufre y el fósforo presentes en ella reaccionan ante el calor de la fricción contra la superficie rugosa de la caja de fósforos.
- Reacciones químicas: Las bases y ácidos de phs extremos generan reacciones de oxidación violenta al tomar contacto con materia orgánica de todo tipo. Es por ello que se advierte del uso de guantes para la manipulación de, por ejemplo, la soda caústica: la piel, así como las mucosas, son materia orgánica y pueden ser dañadas.
- En motores: Los motores de combustión interna utilizan hidrocarburos fósiles, quienes al reaccionar generan pequeñas explosiones que pasarán al sistema de pistones y emergerá del motor como movimiento del automóvil.

