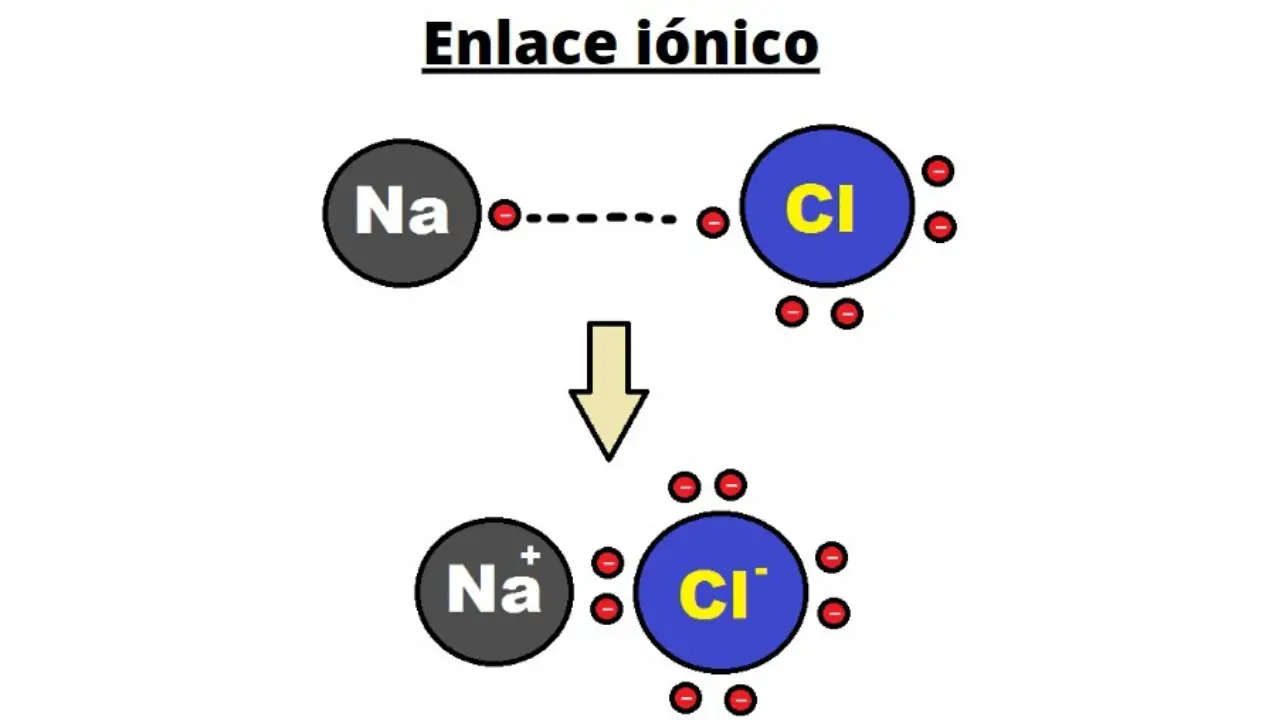
Se llama enlace iónico o enlace electrovalente a aquel enlace químico que se forma cuando un átomo le cede un electrón a otro para llegar a una estabilidad electrónica. Son unos de los tres tipos de enlaces químicos que existen, además de los enlaces covalentes y los enlaces metálicos.
Los enlaces iónicos son los más frecuentes en la formación de compuestos inorgánicos. Este tipo de uniones suele darse en elementos metales y no metales que tengan una electronegatividad diferente o, lo que es lo mismo, que difieren en cuanto a su capacidad para atraer electrones: los metales suelen estar más predispuestos a ceder los electrones mientras que los no metales se muestran dispuestos a aceptarlos.
Cómo se forma un enlace iónico
De lo dicho arriba se desprende que, al aproximarse un elemento metal y uno no metal, busquen estabilizarse eléctricamente, por lo cual el metal dona uno de los electrones de valencia de su capa más externa y el no metal lo recibe en la misma capa.
Una vez hecho esto, ambos elementos cambian de carga: el metal se vuelve positivo y el metal, negativo. Esta diferencia de cargas genera una fuerza de atracción que los ensambla y fortalece el enlace.
¿Por qué iónicos?
El nombre de “enlace iónico” viene dado debido a que, en el proceso de enlace y de intercambio de cargas, acaban formando iones de dos tipos:
- Los cationes, es decir, los iones positivos que pierden un electrón. Los más usuales son los que se forman a partir de metales, pero también existen cationes formados con no metales.
- Y los aniones, que son los iones negativos, puesto que ahora tienen un electrón extra. A la inversa de los cationes, suelen ser más frecuentes los aniones formados por no metales, aunque existen otros mixtos.
Características de los enlaces iónicos
Las características de estas uniones entre átomos tienen que ver con los elementos que las componen, la manera en que se producen y el resultado que forman. En base a esto podemos decir que los enlaces iónicos:
Se originan entre elementos metales (grupos I y II) y no metales (grupos VI y VII) de la tabla periódica, cuyos átomos deben poseer diferente electronegatividad. Esto además significa que, al ser producto de un intercambio de electrones, los átomos resultantes se dividen en cationes y aniones.
Otra característica de estos enlaces es que, debido a la atracción que existe entre cargas negativas y positivas, son enlaces fuertes pero rígidos.
Propiedades de los compuestos
Esta atracción entre cargas hace que los compuestos formados por enlaces iónicos tengan un comportamiento químico particular:
- En estado sólido estos compuestos suelen tener una carga eléctrica neutra.
- Su estructura es tridimensional, lo que hace que se cristalicen fácilmente.
- La fuerza de atracción entre sus iones es tan potente que sus puntos de ebullición y fusión rondan los entre los 300º C y los 1000º C. esto también hace que se mantengan sólidos entre los 20º C y 30º C.
- Si se disuelven en agua, se transforman en excelentes conductores eléctricos.

