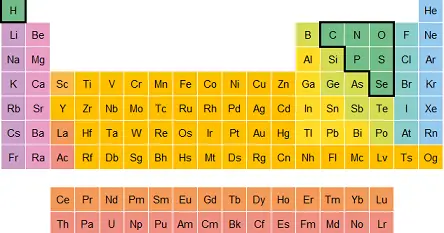
Los no metales son elementos de poca abundancia, ubicados en la sección derecha de la tabla periódica. Se enlazan de forma covalente junto a otros elementos, así como entre ellos mismos. Constituyen elementos esenciales para la vida humana y animal.
Características y propiedades de los No Metales
- Según la clasificación en la que se encuentre el no metal, variará sus propiedades, así como su aspecto o estado de materia en temperatura ambiente. Algunos son sólidos cristalinos, otros amorfos, otros líquidos y algunos están en estado gaseoso. Muchos poseen variantes alotrópicas (mismo elemento con diferente configuración molecular y, por ende, diferentes propiedades y aspectos).
- No son buenos conductores, ni de electricidad ni de calor.
- Puntos de fusión bajos.
- No suelen poseer brillo, aunque sí color, el cual varía según el elemento.
- No son maleables ni dúctiles.
- Al ionizarse adquieren carga negativa (son electronegativos, generando mayor atracción a los electrones que los metales).
- Forma óxidos no metálicos al combinarse con oxígeno.
- La mayoría forma moléculas de dos o más átomos.
- Sus capas electrónicas externas son de alta densidad, por lo que pueden tener variados estados de oxidación (-2,-4,-6,-7,-8).
Clasificación de los No Metales
- Halógenos: Son elementos fuertemente oxidantes, por lo que son altamente electronegativos (tienden a “sacar” electrones frente a otro elemento, oxidando y aumentando el halógeno su carga electrónica). Son tóxicos, poseen un olor característico y en algunos casos pueden presentar carácter metálico. En este grupo están el cloro, el bromo, el flúor, el yodo, el astato y el teneso.
- Gases nobles o inertes: Deben su nombre a su poca nula reactividad química, no tienen propensión a formar moléculas o compuestos frente a otros elementos. En condiciones normales de presión y temperatura son gases monoatómicos. Debido a su inactividad, se producen masivamente para ser aplicados en la industria. Entran en esta categoría el helio, el neón, el radón, el argón, el kriptón, el xenón y el oganesón.
- Otros no metales: Oxígeno, Carbono, Hidrógeno, Azufre, Nitrógeno, Selenio y Fósforo. Estos no metales tienen diversas propiedades. En ejemplos de no metales, veremos más sobre ellos.
Ejemplos de no metales
- Oxígeno: Forma parte del grupo de los anfígenos en la tabla periódica, es altamente reactivo con la mayoría de los elementos, a excepción de los gases nobles. Es el segundo elemento más electronegativo, por debajo del flúor.
- Nitrógeno: Compone el 70% del aire atmosférico, se suele presentar como un gas diatómico en condiciones normales.

Publicidad de Google AdSense
- Carbono: Es abundante en la naturaleza, encontrándose como grafito o diamante también, sus variedades alotrópicas. Es el componente universal de toda forma de vida.
- Hidrógeno: Es el elemento más ligero, siendo un gas inflamable, incoloro, inodoro e insoluble en agua. Constituye más del 70% de la materia visible del universo.
- Flúor: Es un gas verde pálido, muy reactivo y peligroso al contacto con la piel, pudiendo generar quemaduras químicas de gravedad.
Aplicaciones de los No Metales
- Producción de acero: Aleaciones.
- Industrias químicas: Catalizadores, creación de ácidos.
- Industrias alimenticias: Enriquecimiento de productos, uso para procesos intermedios.
- Productos de jardinería: Abonos y fertilizantes.
- Terapias medicinales: Ffarmacología, tratamientos, oncología, medicina nuclear.
- Dataciones nucleares y radiológicas: Investigación y gestión de energía nuclear a través de isótopos.
- Industria petrolífera: Procesos de refinamiento.
Publicidad de Google AdSense

