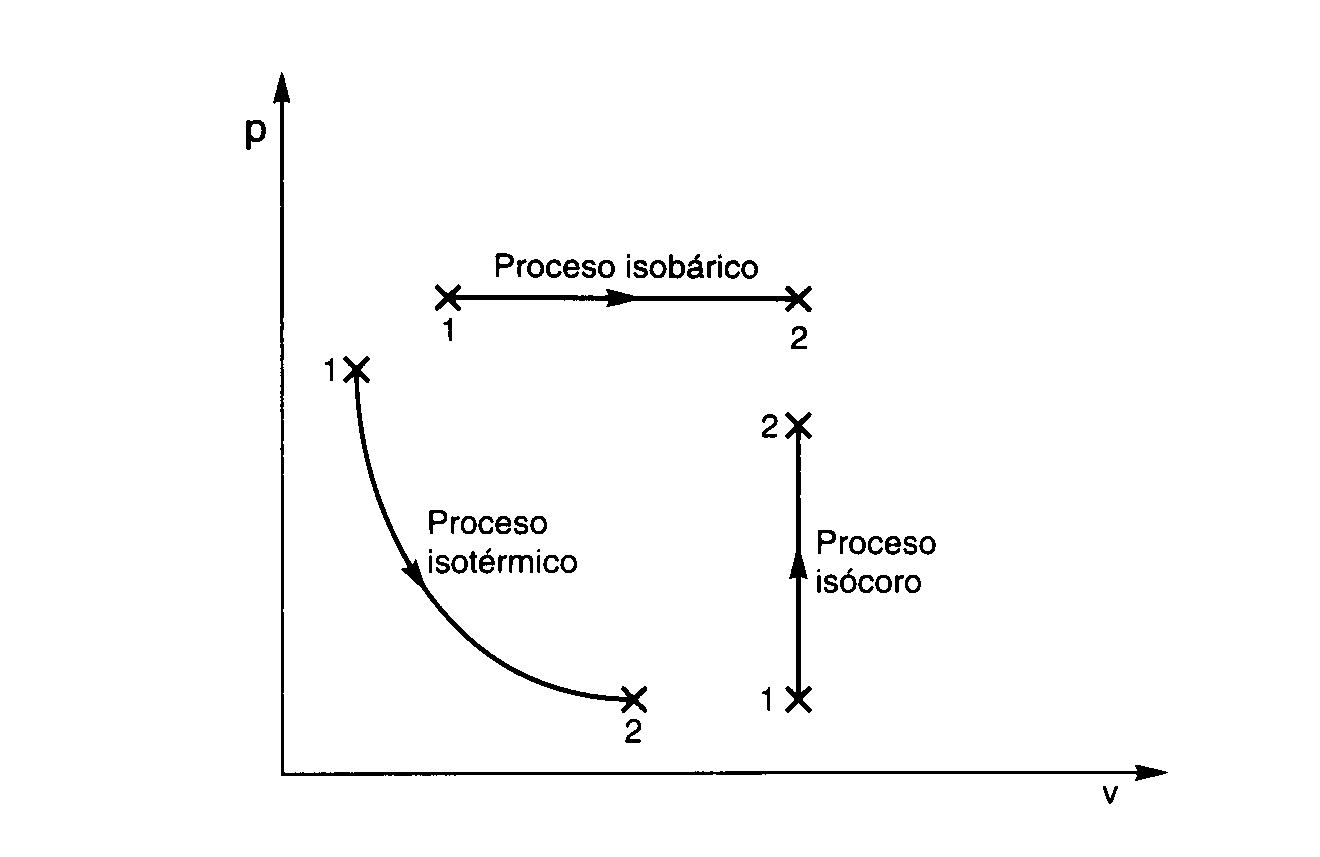
Un proceso isométrico (o también conocido como isocórico o isovolumétrico) es un tipo de proceso termodinámico, en el cual la variante que se mantiene constante es el volumen.
En estos procesos, la presión del gas ideal y su temperatura son directamente proporcionales gracias a la ley de Charles. Cabe aclarar que en los gases reales esta ley no se cumple.
Al graficarse, estos procesos son representados por unas líneas que reciben el nombre de isocoras y que, en el caso de los gases ideales, son rectas en los diagramas que relacionen tres parámetros: T (temperatura), V (volumen) y P (presión).
Fórmulas del proceso isométrico
Existen varias fórmulas relacionadas a estos procesos y que sirven para calcular diferentes cosas.
-
Cálculo del trabajo de un proceso isométrico
En estos procesos no se genera trabajo, ya que el volumen es constante, por lo cual ΔV = 0 y para poder calcular el trabajo entre presión y volumen debemos despejar esta fórmula: W = P·ΔV = P·0
-
Cálculo de la variación de la energía interna de un proceso isométrico
Si aplicamos los principios de la primera ley de la termodinámica, podemos calcular la variación de la energía interna del sistema: ΔU = Q – W.
Pero como no se produce trabajo en estos procesos de volumen constante, el incremento de la energía interna equivale al calor transferido al sistema: ΔU = Q
Si se utiliza una cantidad constante de gas ideal, el aumento de energía será proporcional al crecimiento de temperatura y tensión.
-
Cálculo del calor liberado de un proceso isométrico
Si no cambia la cantidad de gas en el proceso, entonces la variación de energía es proporcional a la variación de la temperatura: Q=n·Cv·ΔT
En esa fórmula podemos encontrar que Cv designa al calor específico molar con volumen constante; la n representa a los moles de gas. ΔT designa a la variación de temperatura durante el proceso.
Ejemplos de procesos isométricos
Veamos algunos ejemplos para comprender mejor los procesos isométricos.
Un ejemplo claro, es el calentar agua en una olla a presión, donde el volumen de agua se mantiene constante, puesto que la olla se encuentra tapada y sin posibilidad de que escape ni una gota de agua. Si se hiciera con una olla normal destapada, estaríamos en presencia de un proceso isobárico, como hemos mencionado en el artículo correspondiente.
Otros ejemplos se producen en ciclos termodinámicos. En este caso podemos mencionar las fases de combustión de la gasolina y la expulsión de gases dentro de los motores de gasolina, son dos procesos isométricos.
Otro ejemplo de este tipo es el ciclo de Stirling: en estos motores, las fases de calentamiento y enfriamiento del gas tienen lugar en un volumen constante, por lo cual se trata de procesos isométricos.

